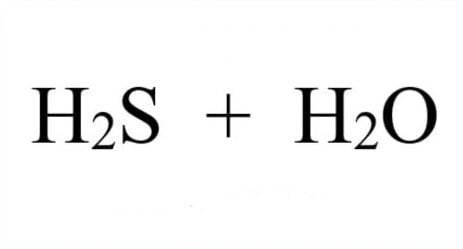
Phản ứng hóa học giữa khí Hydro Sunfua (H2S) khi tác dụng với Nước (H2O), công thức hóa học sẽ được viết như thế nào và sản phẩm tạo ra là chất gì? Hãy cùng Tài Liệu Trọn Đời xem đầy đủ về việc cân bằng phản ứng hóa học H2S + H2O tại đây nhé!
H2S + H2O – Cân bằng phản ứng hóa học
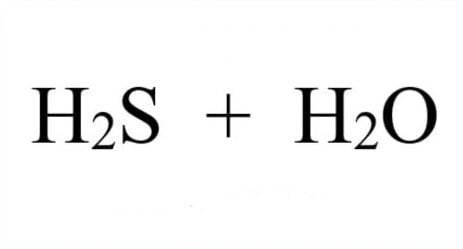
H2S là công thức hóa học của Hydro sulfua, là hỗn hợp khí đã lỏng ở nhiệt độ −60°C, hóa rắn ở nhiệt độ −86°C. H2S dễ ăn mòn và cháy trong điều kiện bình thường.
H2S + 4H2O → H2SO4 + 4H2
Trong đó
- H2S : Hydro sulfua
- H2O : Nước
- H2SO4 : Axít Sunfuric
- H2 : Hydro
Bài tập có chứa H2S và H2O
Bài 1: Cho 2,24 lít khí H2S ở điều kiện tiêu chuẩn phản ứng với dung dịch chứa 0,3 mol KOH. Khối lượng muối tan có trong dung dịch sau phản ứng là bao nhiêu?
A. 11 gam. B. 12 gam.
C. 11,5 gam. D. 10 gam.
Đáp án: A
Bài 2: Cho phản ứng: SO2 + 2H2S → 3S + 2H2O. Câu nào miêu tả đúng tính chất của mỗi chất?
A. SO2 bị oxi hóa và H2S bị khử.
B. SO2 bị khử và H2S bị oxi hóa.
C. SO2 khử H2S và không có chất nào bị oxi hóa.
D. SO2 bị khử, lưu huỳnh bị oxi hóa.
Lời giải
Đáp án: B
Bài 3: Thực hiện thí nghiệm sau: cho khí H2S lưu qua dung dịch CuSO4 thấy có kết tủa màu xám đen xuất hiện, điều này chứng tỏ:
A. Sau phản ứng có kết tủa trắng tạo thành.
B. Có kết tủa CuS tạo thành, không tan trong axit mạnh.
C. Axit sunfuric mạnh hơn axit sunfuahidric.
D. Axit sunfuahidric mạnh hơn axit sunfuaric.
Lời giải
Đáp án: B
Nguồn tham khảo: bierelarue.com.vn