Để hiểu rõ về Cl trong môn hóa học, việc nhớ hóa trị của các nguyên tố trên bảng hệ thống tuần hoàn là rất quan trọng. Trải qua bài học này, chúng ta sẽ tìm hiểu về M của Cl là bao nhiêu và Cl (Clo) hóa trị là bao nhiêu.
Nguyên tử khối của Clo (Cl), M của Clo, Hóa trị Clo
Nguyên tử khối của Clo hay M của Cl là 35,5
Hóa trị của Clo là I,…
Thông tin khác của Clo trong bảng tuần hoàn hóa học:
Ký hiệu hóa học: Cl
Clo thuộc chu kỳ 3 trong bảng tuần hoàn
Số proton: 17
Số nguyên tử bằng 17
Phân loại vào nhóm Halogen
Cấu hình electron [Ne] 3s² 3p⁵
Mỗi lớp chứa 2 7 8 e
Cl có độ âm điện thứ 3 trong tất cả nguyên tố
Tính chất vật lý và hóa học của Clo
Dạng tồn tại của Clo
Clo tồn tại ở dạng lỏng và dạng khí. Clo dưới dạng khí có màu vàng đục, mùi rất khó chịu, độc hại và cần phải sử dụng trang thiết bị bảo hộ khi tiếp xúc trực tiếp.
Công thức hóa học của Clo là Cl2, khối lượng = 71 đvC, nên nặng hơn không khí (32 đvC) khoảng 2.5 lần. Khi Clo ở dạng phân tử, khối lượng là 71, vì vậy Cl nặng hơn nhiều so với không khí. Khí clo tan vừa phải trong nước tạo thành nước clo có màu vàng nhạt và tan nhiều trong dung môi hữu cơ.
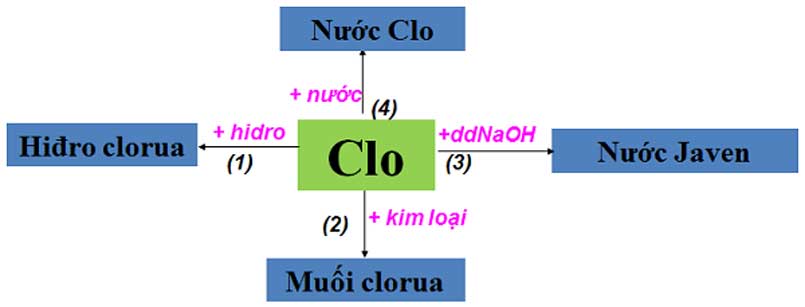
Tác dụng cùng với kim loại
Clo phản ứng với nhiều kim loại để tạo thành muối clorua.
Mg + Cl2 (t°) → MgCl2
2Al + 3Cl2 (t°) → 2AlCl3
Cu + Cl2 (t°) → CuCl2
Fe + Cl2 (t°) → FeCl2
Phản ứng với hidro
Clo phản ứng với hidro để tạo thành khí hidro clorua. Khí hidro clorua tan nhiều trong nước tạo thành axit clohidric.
Cl2 + H2 (t°) → 2HCl ↑
Bạn đang đọc: Cl có nguyên tử khối bao nhiêu?
Phản ứng với nước
Khí clo phản ứng với nước để tạo ra dung dịch nước clo.
Cl2 + H2O ⇔ HCl + HClO
Dung dịch nước clo chứa các chất: Cl2, HCl, HClO và nước. Nó có màu vàng nhạt và mùi hắc. Ban đầu, dung dịch nước clo làm thay đổi màu của giấy quỳ tím từ tím sang đỏ, sau đó mất màu do HClO có khả năng oxi hóa mạnh.
Phản ứng với dung dịch NaOH
Khí clo tác dụng với dung dịch NaOH để tạo ra dung dịch nước Gia-ven. Đây là dung dịch có tính oxi hóa mạnh, làm thay đổi màu giấy quỳ tím.
Cl2 + 2NaOH → NaCl + NaClO + H2O
Kết luận
Trên đây, Tài Liệu Trọn Đời đã chia sẻ đến các bạn về M của Clo cũng như hóa trị của Cl (Clo). Nếu bạn thấy bài viết hữu ích, hãy chia sẻ cho bạn bè của mình nhé.